関節リウマチ治療薬としてのJAK阻害薬の現状と課題
JAK阻害薬は生物学的製剤と同様の有効性を持つ薬剤として位置付けされます。現在(2021年12月)処方可能な5つのJAK阻害薬はそれぞれ代謝経路・排泄経路が異なるため個々の肝・腎機能に応じた使い分けが必要です。また生物学的製剤と比べて重篤な感染症発症リスクに差はありませんが、帯状疱疹がややおこりやすいという報告があります。しかし、長期的な安全性についてのエビデンスは従来の抗リウマチ薬に比べてまだ少なく、市販後調査も完全に終わっていないことから慎重な経過観察が必要と思われます。
(JAK阻害薬とは)
細胞の外から様々な刺激を細胞内に伝えるために働く酵素群はkinase(キナーゼ)と呼ばれ 数多くの種類が存在しますが、JAKはこのうちの一つであるJanus kinase(ヤヌスキナーゼ)の略称でJAK1, JAK2, JAK3, TYK2の4種類があります。
関節リウマチでは炎症が起きている関節内に白血球など免疫に関与する細胞が多数見られますが、サイトカインという物質がこれらの細胞を活性化して炎症をひきおこしています。サイトカインは細胞の表面にあるサイトカイン受容体に結合することにより細胞に刺激を与えますが、さらにその刺激は細胞内に伝わって細胞の中心にある核に到達します。その結果、核内ではDNA合成が盛んに行なわれ細胞が増えたり炎症を起こす様々な物質を作ったりするようになります。JAKは細胞の中でサイトカイン受容体に結合し、サイトカインによる刺激を下流に伝える重要なkinase(キナーゼ)です(1)。
JAK阻害薬はサイトカイン受容体からの刺激を細胞の中で遮断することにより複数の種類のサイトカインをブロックして炎症を抑えます(JAK阻害薬は飲み薬です)。
これに対し生物学的製剤はそれぞれの薬剤が1種類の特定のサイトカインを細胞の外でブロックすることにより細胞に炎症を起こす刺激が入らないようにします(生物学的製剤は注射薬です)。
(関節リウマチ治療においてJAK阻害薬が占める位置)
JAK阻害薬がリウマチ医療の現場に登場してから約8年が経過しました( Topics, 2013.07.16 を参照 )。
有効性や安全性の面で依然未解明の部分が残されていますが、5種類のJAKが使えるようになった現在、関節リウマチ治療におけるJAK阻害薬の占める位置が若干変化して来ました。
関節リウマチの治療指針であるEULAR(欧州リウマチ学会)リコメンデーションの2019年版(2) を1つ前の2016年版(3)と比較してみますと 2016年版では予後不良因子を有する患者のメトトレキサート(MTX)効果不十分例に対して生物学的製剤またはJAK阻害薬を使用することを推奨していましたが、生物学的製剤のほうがやや優先順位が高くなっていました。それが2019年版では両者の扱いが同等になりました。これはJAK阻害薬の長期的有効性や安全性のエビデンスがでて生物学的製剤と優劣をつけることができなくなったためです。
また日本では2014年から6年ぶりに改訂された「関節リウマチ診療ガイドライン2020(4)」において治療のスタンダードとして新たにJAK阻害薬が付け加えられ、JAK阻害薬(トファシチニブ、バリシチニブ、ペフィシチニブの3剤)に関する5項目にわたる推奨が新設されました(表1)。
表1. JAK阻害薬に関する推奨(4)

そしてMTXや生物学的製剤で効果不十分な例に対してはMTXとの併用や単独での投与を条件付きで推奨しつつも長期の安全性が十分に確立されてない点を考慮する必要があるとしています。またJAK阻害薬で寛解もしくは低疾患活動性を維持している患者には条件付きで減量を推奨しています。
(JAK阻害薬の安全性と課題)
いずれのJAK阻害薬も細胞内のシグナル伝達を阻害するために複数のサイトカインをブロックする効果があり、長期的な安全性に関する懸念は生物学的製剤よりも少ないとは言えません。経口薬(飲み薬)であるがゆえの安易な使用は避け、使用前のスクリーニング、使用中のモニタリングは徹底すべきです。
①それぞれの薬物の代謝・排泄経路を考える
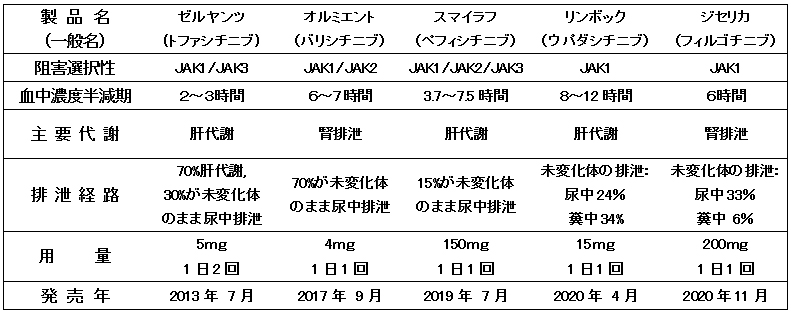
関節リウマチの患者は高齢者の割合が高く、肝・腎機能が低下している場合 薬物排泄遅延による薬物血中濃度の上昇(薬物が体の中に残る)がおこることがあります。この場合予期せぬ副作用が出現することも考えられます。現在処方可能な5種類のJAK阻害薬はそれぞれ肝代謝、腎排泄の割合が異なる(表2)ので しっかり理解したうえで使用する必要があります。
②感染症の合併リスク(とくに帯状疱疹)
使用中に重篤な感染症を合併する頻度は生物学的製剤と同じ程度とされていますが(5)、帯状疱疹に関してはJAK阻害薬の投与を受けている場合やや多いことが報告されています(6)(7)(トファシチニブの市販後調査では9.2/100人の報告があります)。このためJAK阻害薬導入時に帯状疱疹ワクチンの接種を検討する必要があります。
③悪性腫瘍との関連
JAK阻害薬は腫瘍免疫において重要な役割を果すIL-15というサイトカインを阻害する働きがあるので悪性腫瘍が増えるのではないかということが当初懸念されました。現在までの所、JAK阻害薬により悪性腫瘍が増えたという報告はありません(8)(9)。しかし長期的な安全性についてのエビデンスは従来の抗リウマチ薬に比べてまだ少なく、市販後調査の結果も完全に出ていないことから慎重な経過観察が必要です。
表2. JAK阻害薬の比較
・JAK1は炎症性サイトカインシグナルにおいて重要
・JAK2は赤血球成熟にとって重要
・JAK3シグナルは免疫監視およびリンパ球機能において重要
(参考文献)
(1) Tanaka Y, et al. In vitro and in vivo analysis of a JAK inhibitor in rheumatoid arthritis.
Ann Rheum Dis. 71: 70 – 74, 2012
(2) Swolen JS, et al. EULAR recommendation for the management of rheumatoid arthritis
with synthetic and biological disease modifying antirheumatic drugs : 2019 update.
Ann Rheum Dis. 79 : 685 – 699, 2020
(3) Swolen JS, et al. EULAR recommendation for the management of rheumatoid arthritis
with synthetic and biological disease-modiying antirheumatic drugs: 2016 update.
Ann Rheum Dis. 76: 948 – 959, 2017
(4) 関節リウマチ診療ガイドライン2020, 一般社団法人日本リウマチ学会編集、診断と治療社
(5) Cohen S, et al. Analysis of infections and all-cause mortality in phase Ⅱ, phase Ⅲ, and
long-term extension studies of tofacitinib in patients with rheumatoid arthritis. Arthritis
Rheumatol. 66: 2924 – 2937, 2014
(6) Yamaoka K. Benefit and risk of Tofacitinib in the treatment of rheumatoid arthritis:
A focus on Herpes Zoster. Drug Saf. 39: 823 – 840, 2016
(7) Curtis JR, et al. Risk for Herpes Zoster in Tofacitinib-treated rheumatoid arthritis patients
with and without concominant methotrexate and glucocorticoids. Arthritis Care Res.
71(9): 1249 – 1254, 2019
(8) Curtis JR, et al. Tofacitinib, an oral Janus kinase inhibitor: analysis of malignancies across
the rheumatoid arthritis clinical development programme. Ann Rheum Dis. 75(5): 831 –
841, 2016
(9) Sivaraman P and Cohen SB Malignancy and Janus kinase inhibition. Rheum Dis Clin North
Am. 43(1): 79 – 93, 2017
(2021.12.27)